Чтобы научиться составлять электронно-графические формулы, важно понять теорию строения атомного ядра. Ядро атома составляют протоны и нейтроны. Вокруг ядра атома на электронных орбиталях находятся электроны.
Вам понадобится
- — ручка;
- — бумага для записей;
- — периодическая система элементов (таблица Менделеева).
Инструкция
Электроны в атоме занимают свободные орбитали в последовательности, называемой шкалой энергии:1s / 2s, 2p / 3s, 3p / 4s, 3d, 4p / 5s, 4d, 5p / 6s, 4d, 5d, 6p / 7s, 5f, 6d, 7p. На одной орбитали могут располагаться два электрона с противоположными спинами – направлениями вращения.
Структуру электронных оболочек выражают с помощью графических электронных формул. Для записи формулы используйте матрицу. В одной ячейке могут располагаться один или два электрона с противоположными спинами. Электроны изображаются стрелками. Матрица наглядно показывает, что на s-орбитали могут располагаться два электрона, на p-орбитали – 6, на d – 10, на f -14.
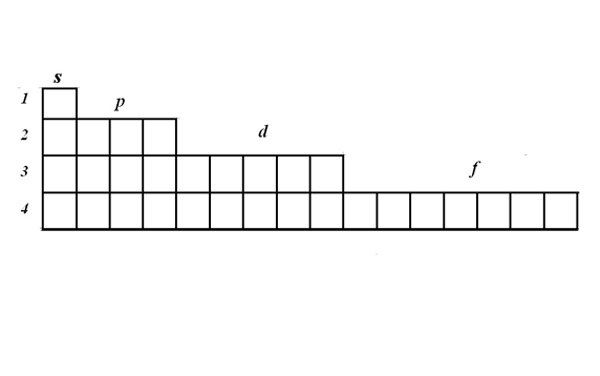
Рассмотрите принцип составления электронно-графической формулы на примере марганца. Найдите марганец в таблице Менделеева. Его порядковый номер 25, значит в атоме 25 электронов, это элемент четвертого периода.
Запишите порядковый номер и символ элемента рядом с матрицей. В соответствии со шкалой энергии заполоните последовательно 1s, 2s, 2p, 3s, 3p, 4s уровни, вписав по два электрона в ячейку. Получится 2+2+6+2+6+2=20 электронов. Эти уровни заполнены полностью.
У вас осталось еще пять электронов и незаполненный 3d-уровень. Расположите электроны в ячейках d-подуровня, начиная слева. Электроны с одинаковыми спинами расположите в ячейках сначала по одному. Если все ячейки заполнены, начиная слева, добавьте по второму электрону с противоположным спином. У марганца пять d-электронов, расположенных по одному в каждой ячейке.
Электронно-графические формулы наглядно показывают количество неспаренных электронов, которые определяют валентность.
При создании теоретических и практических работ по математике, физике, химии студент или школьник сталкивается с необходимостью вставки специальных символов и сложных формул. Располагая приложением Word из офисного пакета Microsoft, можно набрать электронную формулу любой сложности.
Инструкция
Откройте новый документ в Microsoft Word. Присвойте ему название и сохраните в той же папке, где у вас лежит работа, чтобы в будущем не искать.
Перейдите на вкладку «Вставка». Справа найдите символ?, а рядом надпись «Формула». Нажмите на стрелочку. Появится окно, в котором вы можете выбрать встроенную формулу, например, формулу квадратного уравнения.
Нажмите на стрелку и на верхней панели появятся самые разные символы, которые вам могут понадобиться при написании конкретно этой формулы. Изменив ее так, как нужно вам, вы можете сохранить ее. С этого момента она будет выпадать в списке встроенных формул.
Если вам нужно перенести формулу в текст, который позже нужно разместить на сайте, то кликните на активном поле с ней правой кнопкой мыши и выберите не профессиональный, а линейный способ написания. В частности, формула все того же квадратного уравнения в данном случае примет вид:x=(-b±?(b^2-4ac))/2a.
Другой вариант написания электронной формулы в Word – через конструктор. Зажмите одновременно клавиши Alt и=. У вас сразу появится поле для написания формулы, а в верхней панели откроется конструктор. Здесь вы можете выбрать все знаки, которые могут понадобиться для записи уравнения и решения любой задачи.
Некоторые символы линейной записи могут быть непонятными читателю, незнакомому с компьютерной символикой. В этом случае самые сложные формулы или уравнения имеет смысл сохранить в графическом виде. Для этого откройте самый простой графический редактор Paint: «Пуск» — «Программы» — «Paint». Затем увеличьте масштаб документа с формулой так, чтобы она заняла весь экран. Это необходимо, чтобы сохраненное изображение имело наибольшее разрешение. Нажмите на клавиатуре PrtScr, перейдите в Paint и нажмите Ctrl+V.
Обрежьте все лишнее. В итоге у вас получится качественное изображение с нужной формулой.
Обратите внимание
Помните, что химия – наука исключений. У атомов побочных подгрупп Периодической системы встречается «проскок» электрона. Например, у хрома с порядковым номером 24 один из электронов с 4s-уровня переходит в ячейку d-уровня. Похожий эффект есть у молибдена, ниобия и др. Кроме того, есть понятие возбужденного состояния атома, когда спаренные электроны распариваются и переходят на соседние орбитали. Поэтому при составлении электронно-графических формул элементов пятого и последующих периодов побочной подгруппы сверяйтесь со справочником.
Электронное строение атома можно показать электронной формулой и электронно-графической схемой. В электронных формулах последовательно записываются энергетические уровни и подуровни в порядке их заполнения и общее число электронов на подуровне. При этом состояние отдельного электрона, в частности его магнитное и спиновое квантовые числа, в электронной формуле не отражено. В электронно-графических схемах каждый электрон «виден» полностью, т.е. его можно охарактеризовать всеми четырьмя квантовыми числами. Электронно-графические схемы обычно приводятся для внешних электронов.
Пример 1. Напишите электронную формулу фтора, состояние внешних электронов выразите электронно-графической схемой. Сколько неспаренных электронов в атоме этого элемента?
Решение. Атомный номер фтора равен девяти, следовательно, в его атоме имеется девять электронов. В соответствии с принципом наименьшей энергии, пользуясь рис. 7 и учитывая следствия принципа Паули, записываем электронную формулу фтора: 1s 2 2s 2 2p 5 . Для внешних электронов (второй энергетический уровень) составляем электронно-графическую схему (рис. 8), из которой следует, что в атоме фтора имеется один неспаренный электрон.
Рис. 8. Электронно-графическая схема валентных электронов атома фтора
Пример 2. Составьте электронно-графические схемы возможных состояний атома азота. Какие из них отражают нормальное состояние, а какие – возбужденное?
Решение. Электронная формула азота 1s 2 s 2 2p 3 , формула внешних электронов: 2s 2 2p 3 . Подуровень 2p незавершен, т.к. число электронов на нем меньше шести. Возможные варианты распределения трех электронов на 2р-подуровне показаны на рис. 9.
Рис. 9. Электронно-графические схемы возможных состояний 2р-подуровня в атоме азота.
Максимальное (по абсолютной величине) значение спина (3 / 2) соответствует состояниям 1 и 2, следовательно, они являются основными, а остальные – возбужденные.
Пример 3. Определите квантовые числа, которыми определяется состояние последнего электрона в атоме ванадия?
Решение. Атомный номер ванадия Z=23, следовательно, полная электронная формула элемента: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 3 . Электронно-графическая схема внешних электронов (4s 2 3d 3) такова (рис. 10),:
Рис. 10. Электронно-графическая схема валентных электронов атома ванадия
Главное квантовое число последнего электрона n=3 (третий энергетический уровень), орбитальное l =2 (подуровень d). Mагнитное квантовое число для каждого из трех d-электронов различно: для первого оно равно –2, для второго –1, для третьего – 0. Спиновое квантовое число у всех трех электронов одинаково: m s=+ 1 / 2 . Таким образом, состояние последнего электрона в атоме ванадия характеризуется квантовыми числами: n=3; l=2; m=0; m s=+ 1 / 2 .
7. Спаренные и неспаренные электроны
Электроны, заполняющие орбитали попарно, называются спаренными, а одиночные электроны называются неспаренными . Неспаренные электроны обеспечивают химическую связь атома с другими атомами. Наличие неспаренных электронов устанавливается экспериментально изучением магнитных свойств. Вещества с неспаренными электронами парамагнитны (втягиваются в магнитное поле благодаря взаимодействию спинов электронов, как элементарных магнитов, с внешним магнитным полем). Вещества, имеющие только спаренные электроны, диамагнитны (внешнее магнитное поле на них не действует). Неспаренные электроны находятся только на внешнем энергетическом уровне атома и их число можно определить по его электронно-графической схеме.
Пример 4. Определите число неспаренных электронов в атоме серы.
Решение. Атомный номер серы Z=16, следовательно, полная электронная формула элемента: 1s 2 2s 2 2p 6 3s 2 3p 4 . Электронно-графическая схема внешних электронов такова (рис. 11).
Рис. 11. Электронно-графическая схема валентных электронов атома серы
Из электронно-графической схемы следует, что в атоме серы имеется два неспаренных электрона.
При написании электронных формул атомов элементов указывают энергетические уровни (значения главного квантового числа n в виде цифр – 1, 2, 3 и т.д.), энергетические подуровни (значения орбитального квантового числа l в виде букв – s , p , d , f ) и цифрой вверху указывают число электронов на данном подуровне.
Первым элементом в таблице Д.И. Менделеева является водород, следовательно, заряд ядра атома Н равен 1, в атоме только один электрон на s -подуровне первого уровня. Поэтому электронная формула атома водорода имеет вид:
Вторым элементом является гелий, в его атоме два электрона, поэтому электронная формула атома гелия – 2 Не 1s 2 . Первый период включает в себя только два элемента, так как заполняется электронами первый энергетический уровень, который могут занять только 2 электрона.
Третий по порядку элемент – литий – находится уже во втором периоде, следовательно, у него начинает заполняться электронами второй энергетический уровень (об этом мы говорили выше). Заполнение электронами второго уровня начинается с s -подуровня, поэтому электронная формула атома лития – 3 Li 1s 2 2s 1 . В атоме бериллия завершается заполнение электронами s -подуровня: 4 Ве 1s 2 2s 2 .
У последующих элементов 2-го периода продолжает заполняться электронами второй энергетический уровень, только теперь электронами заполняется р -подуровень: 5 В 1s 2 2s 2 2р 1 ; 6 С 1s 2 2s 2 2р 2 … 10 Ne 1s 2 2s 2 2р 6 .
У атома неона завершается заполнение электронами р -подуровня, этим элементом заканчивается второй период, в нем восемь электронов, так как на s — и р -подуровнях могут находиться только восемь электронов.
У элементов 3-го периода имеет место аналогичная последовательность заполнения электронами энергетических подуровней третьего уровня. Электронные формулы атомов некоторых элементов этого периода имеют вид:
11 Na 1s 2 2s 2 2р 6 3s 1 ; 12 Mg 1s 2 2s 2 2р 6 3s 2 ; 13 Al 1s 2 2s 2 2р 6 3s 2 3p 1 ;
14 Si 1s 2 2s 2 2р 6 3s 2 3p 2 ;…; 18 Ar 1s 2 2s 2 2р 6 3s 2 3p 6 .
Третий период, как и второй, заканчивается элементом (аргоном), у которого завершается заполнение электронами р –подуровня, хотя третий уровень включает в себя три подуровня (s , р , d ). Согласно приведенному выше порядку заполнения энергетических подуровней в соответствии с правилами Клечковского, энергия подуровня 3d больше энергии подуровня 4s , поэтому у следующего за аргоном атома калия и стоящего за ним атома кальция заполняется электронами 3s –подуровень четвертого уровня:
19 К 1s 2 2s 2 2р 6 3s 2 3p 6 4s 1 ; 20 Са 1s 2 2s 2 2р 6 3s 2 3p 6 4s 2 .
Начиная с 21-го элемента – скандия, в атомах элементов начинает заполняться электронами подуровень 3d . Электронные формулы атомов этих элементов имеют вид:
21 Sc 1s 2 2s 2 2р 6 3s 2 3p 6 4s 2 3d 1 ; 22 Ti 1s 2 2s 2 2р 6 3s 2 3p 6 4s 2 3d 2 .
В атомах 24-го элемента (хрома) и 29-го элемента (меди) наблюдается явление, называемое «проскоком» или «провалом» электрона: электрон с внешнего 4s –подуровня «проваливается» на 3d –подуровень, завершая заполнение его наполовину (у хрома) или полностью (у меди), что способствует бóльшей устойчивости атома:
24 Cr 1s 2 2s 2 2р 6 3s 2 3p 6 4s 1 3d 5 (вместо …4s 2 3d 4) и
29 Cu 1s 2 2s 2 2р 6 3s 2 3p 6 4s 1 3d 10 (вместо …4s 2 3d 9).
Начиная с 31-го элемента – галлия, продолжается заполнение электронами 4-го уровня, теперь – р –подуровня:
31 Ga 1s 2 2s 2 2р 6 3s 2 3p 6 4s 2 3d 10 4p 1 …; 36 Кr 1s 2 2s 2 2р 6 3s 2 3p 6 4s 2 3d 10 4p 6 .
Этим элементом и завершается четвертый период, который включает в себя уже 18 элементов.
Аналогичный порядок заполнения электронами энергетических подуровней имеет место в атомах элементов 5-го периода. У первых двух (рубидия и стронция) заполняется s –подуровень 5-го уровня, у последующих десяти элементов (с иттрия по кадмий) заполняется d –подуровень 4-го уровня; завершают период шесть элементов (с индия по ксенон), в атомах которых происходит заполнение электронами р –подуровня внешнего, пятого уровня. В периоде тоже 18 элементов.
У элементов шестого периода такой порядок заполнения нарушается. В начале периода, как обычно, находятся два элемента, в атомах которых заполняется электронами s –подуровень внешнего, шестого, уровня. У следующего за ними элемента – лантана – начинает заполняться электронами d –подуровень предыдущего уровня, т.е. 5d . На этом заполнение электронами 5d -подуровня прекращается и у следующих 14 элементов – с церия по лютеций – начинает заполняться f -подуровень 4-го уровня. Эти элементы включены все в одну клетку таблицы, а внизу приведен развернутый ряд этих элементов, называемых лантаноидами.
Начиная с 72-го элемента – гафния – по 80-й элемент – ртуть, продолжается заполнение электронами 5d –подуровня, и завершается период, как обычно шестью элементами (с таллия по радон), в атомах которых заполняется электронами р –подуровень внешнего, шестого, уровня. Это самый большой период, включающий в себя 32 элемента.
В атомах элементов седьмого, незавершенного, периода просматривается тот же порядок заполнения подуровней, что описан выше. Предоставляем студентам самим написать электронные формулы атомов элементов 5 – 7-го периодов с учетом всего сказанного выше.
Примечание: в некоторых учебных пособиях допускается другой порядок записи электронных формул атомов элементов: не в порядке их заполнения, а в соответствии с приводимым в таблице количеством электронов на каждом энергетическом уровне. Например, электронная формула атома мышьяка может иметь вид: As 1s 2 2s 2 2р 6 3s 2 3p 6 3d 10 4s 2 4p 3 .
Согласно представлениям Гейтлера и Лондона, валентность элементов определяется числом неспаренных электронов. Рассмотрим электронно-графические формулы некоторых элементов, в которых орбитали представляют в виде ячеек- квадратов, а электрон в виде стрелок + ½; -1/2.
Из этих формул следует, что в нормальном (неспаренном) состоянии углерод имеет II валентность, Sc – I.Атомы могут переходить в возбуждённое состояние, при котором с ниже лежащих подуровней могут переходить выше лежащие пустые подуровне (в пределах одного подуровня).
6. Периодический закон и периодическая система д.И. Менделеева Структура периодической системы (период, группа, подгруппа). Значение периодического закона и периодической системы.
Периодический закон Д. И. Менделеева: Свойства простых тел , а также формы и свойства соеди нений элементов находятся в периодической зависимости от величины атомных весов элементов .(Свойства эл-тов находятся в периодической зависимости от заряда атомов их ядер).
Периодическая система элементов. Ряды элементов, в пределах которых свойства изменяются последовательно, как, например, ряд из восьми элементов от лития до неона или от натрия до аргона, Менделеев назвал периодами. Если напишем эти два периода один под другим так, чтобы под литием находился натрий, а под неоном — аргон, то получим следующее расположение элементов:
При таком расположении в вертикальные столбцы попадают элементы, сходные по своим свойствам и обладающие одинаковой валентностью, например, литий и натрий, бериллий и магний и т. д.
Разделив все элементы на периоды и располагая один период под другим так, чтобы Сходные по свойствам и типу образуемых соединений элементы приходились друг под другом, Менделеев составил таблицу, названную им периодической системой элементов по группам и рядам.
Значение периодической систе мы. Периодическая система элементов оказала большое влияние на последующее развитие химии. Она не только была первой естественной классификацией химических элементов, показавшей, что они образуют стройную систему и находятся в тесной связи друг с другом, но и явилась могучим орудием для дальнейших исследований.
7. Периодическое изменение свойств химических элементов. Атомные и ионные радиусы. Энергия ионизации. Сродство к электрону. Электроотрицательность.
Зависимость атомных радиусов от заряда ядра атома Z имеет периодический характер. В пределах одного периода с увеличением Z проявляется тенденция к уменьшению размеров атома, что особенно четко наблюдается в коротких периодах
С началом застройки нового электронного слоя, более удаленного от ядра, т. е. при переходе к следующему периоду, атомные радиусы возрастают (сравните, например, радиусы атомов фтора и натрия). В результате в пределах подгруппы с возрастанием заряда ядра размеры атомов увеличиваются.
Потеря атомов электронов приводит к уменьшению его эффективных размеров, а присоединение избыточных электронов — к увеличению. Поэтому радиус положительно заряженного иона (катиона) всегда меньше, а радиус отрицательно заряженного нона (аниона) всегда больше радиуса соответствующего электронейтрального атома.
В пределах одной подгруппы радиусы ионов одинакового заряда возрастают с увеличением заряда ядра Такая закономерность объясняется увеличением числа электронных слоев и растущим удалением внешних электронов от ядра.
Наиболее характерным химическим свойством металлов является способность их атомов легко отдавать внешние электроны и превращаться в положительно заряженные ионы, а неметаллы, наоборот, характеризуются способностью присоединять электроны с образованием отрицательных ионов. Для отрыва электрона от атома с превращением последнего в положительный ион нужно затратить некоторую энергию, называемую энергией ионизации.
Энергию ионизации можно определить путем бомбардировки атомов электронами, ускоренными в электрическом поле. То наименьшее напряжение поля, при котором скорость электронов становится достаточной для ионизации атомов, называется потенциалом ионизации атомов данного элемента и выражается в вольтах.
При затрате достаточной энергии можно оторвать от атома два, три и более электронов. Поэтому говорят о первом потенциале ионизации (энергия отрыва от атома первого электрона).втором потенциале ионизации (энергия отрыва второго электрона)
Как отмечалось выше, атомы могут не только отдавать, но и присоединять электроны. Энергия, выделяющаяся при присоединении электрона к свободному атому, называется сродством атома к электрону. Сродство к электрону, как и энергия ионизации, обычно выражается в электронвольтах. Так, сродство к электрону атома водорода равно 0,75 эВ, кислорода-1,47 эВ, фтора -3,52 эВ.
Сродство к электрону атомов металлов, как правило, близко к нулю или отрицательно; из этого следует, что для атомов большинства металлов присоединение электронов энергетически невыгодно. Сродство же к электрону атомов неметаллов всегда положительно и тем больше, чем ближе к благородному газу расположен неметалл в периодической системе; это свидетельствует об усилении неметаллических свойств по мере приближения к концу периода.
| » |
ОПРЕДЕЛЕНИЕ
Электронная формула (конфигурация) атома химического элемента показывает расположение электронов на электронных оболочках (уровнях и подуровнях) в атоме или молекуле.
Наиболее часто электронные формулы записывают для атомов в основном или возбужденном состоянии и для ионов.
Существует несколько правил, которые необходимо учитывать при составлении электронной формулы атома химического элемента. Это принцип Паули, правила Клечковского или правило Хунда.
Составление электронной и электронно-графической формулы
При составление электронной формулы следует учитывать, что номер периода химического элемента определяет число энергетических уровней (оболочек) в атоме, а его порядковый номер количество электронов.
Согласно правилу Клечковского , заполнение энергетических уровней происходит в порядке возрастания суммы главного и орбитального квантовых чисел (n + l), а при равных значениях этой суммы — в порядке возрастания n:
1s < 2s < 2p < 3s < 3p < 4s ≈ 3d < 4p < 5s ≈ 4d < 5p < 6s ≈ 5d ≈ 4f < 6p и т.д.
Так, значению n + l=5 соответствуют энергетические подуровни 3d (n=3, l=2), 4d (n=4, l=1) и 5s (n=5, l=0). Первым из этих подуровней заполняется тот, у которого ниже значение главного квантового числа.
Поведение электронов в атомах подчиняется принципу запрета, сформулированному швейцарским ученым В. Паули: в атоме не может быть двух электронов, у которых были бы одинаковыми все четыре квантовых числа. Согласно принципу Паули , на одной орбитали, характеризуемой определенными значениями трех квантовых чисел (главное, орбитальное и магнитное), могут находиться только два электрона, отличающиеся значением спинового квантового числа. Из принципа Паули вытекает следствие : максимально возможное число электронов на каждом энергетическом уровне равно удвоенному значению квадрата главного квантового числа.
Электронную формулу атома изображают следующим образом: каждому энергетическому уровню соответствует определенное главное квантовое число n, обозначаемое арабской цифрой; за каждой цифрой следует буква, соответствующая энергетическому подуровню и обозначающая орбитальное квантовое число. Верхний индекс у буквы показывает число электронов, находящихся в подуровне. Например, электронная формула атома натрия имеет следующий вид:
11 N 1s 2 2s 2 2p 6 3s 1 .
При заполнение электронами энергетических подуровней также необходимо соблюдать правило Хунда : в данном подуровне электроны стремятся занять энергетические состояния таким образом, чтобы суммарный спин был максимальным, что наиболее наглядно отражается при составлении электронно-графических формул.
Электронно-графические формулы обычно изображают для валентных электронов. В такой формуле все электроны помечаются стрелочками, а ячейками (квадратиками) — орбитали. В одной ячейке не может находиться более двух электронов. Рассмотрим на примере ванадия. Сначала записываем электронную формулу и определяем валентные электроны:
74 W) 2) 8) 18) 32) 12) 2 ;
1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 4f 14 5s 2 5p 6 5d 4 6s 2 .
Внешний энергетический уровень атома вольфрама содержит 6 электронов, которые являются валентными. Энергетическая диаграмма основного состояния принимает следующий вид:
Примеры решения задач
ПРИМЕР 1
| Задание | Изобразите электронную и электронно-графическую формулу химического элемента алюминия. |
| Ответ | Алюминий имеет порядковый номер 13 и расположен в третьем периоде Периодической системы Д.И. Менделеева, следовательно, атом этого химического элемента состоит из положительно заряженного ядра, внутри которого находится 13 протонов, а вокруг ядра имеется три оболочки, по которым движутся 13 электронов.
Электронная формула алюминия выглядит следующим образом: 13 Al) 2) 8) 3 ; 1s 2 2s 2 2p 6 3s 2 3p 1 . На внешнем энергетическом уровне алюминия находится три электрона, все электроны 3-го подуровня. Электронно-графическая формула имеет следующий вид: |